- · 光谱学与光谱分析版面费[04/09]
- · 《光谱学与光谱分析》投[04/09]
- · 《光谱学与光谱分析》数[04/09]
浅谈光谱学和光谱测定法
作者:网站采编关键词:
摘要:简介:光谱学是研究能量和物质之间作为波长函数的相互作用。不同的化学元素具有不同的发射线特性,因此可以通过分析光谱线来推断未知物体的化学成分。光子的能量与其波长有关
简介:光谱学是研究能量和物质之间作为波长函数的相互作用。不同的化学元素具有不同的发射线特性,因此可以通过分析光谱线来推断未知物体的化学成分。光子的能量与其波长有关,因此光谱学可用于识别任何化学元素或化合物。
光谱学是研究能量和物质之间作为波长函数的相互作用。不同的化学元素具有不同的发射线特性,因此可以通过分析光谱线来推断未知物体的化学成分。光子的能量与其波长有关,因此光谱学可用于识别任何化学元素或化合物。
在了解什么是光谱之前,我们先来了解一下什么是光。光是一种电磁波 (EM)。
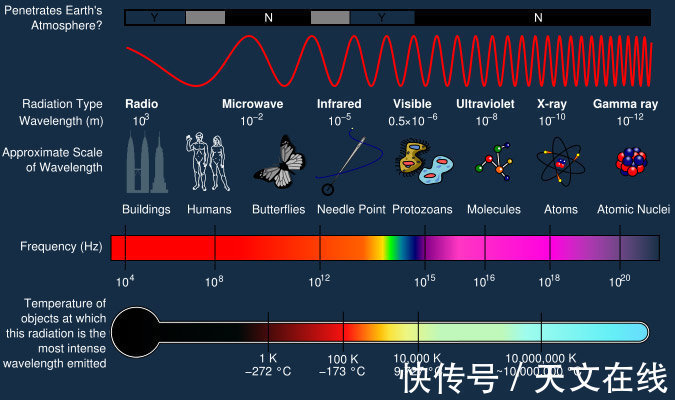
电磁波谱
这对于文章中,我们只需要关注可见光。
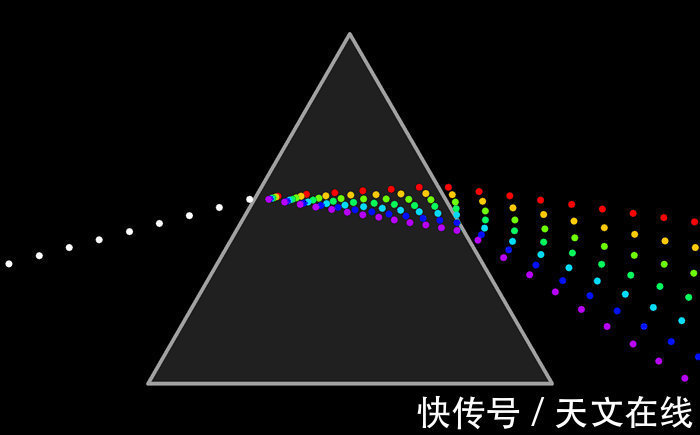
光通过棱镜的动画演示
早在公元 40 世纪,塞纳卡就发现了光通过棱镜的色散。然而,直到牛顿于 1666 年提出由不同颜色组成的尾灯概念,这一概念才广为流传。 1802年,英国化学家威廉·海德·沃拉斯顿从玻璃棱镜中观察到光谱中的暗线(吸收线)。后来,在 1814 年,德国物理学家约瑟夫·冯·弗劳恩霍夫(Joseph von Fraunhofer)独立地重新发现了这些谱线,并开始系统地研究这些波长的特性。他一共画了570多条线,从A到K,较弱的线用其他字母表示。

可见光谱中的氢吸收谱线
如果你通过棱镜观察太阳光谱,你或许可以观察到上图。这些被称为弗劳恩霍夫线或吸收线。
1859年,古斯塔夫·罗伯特·基尔霍夫(Gustav Robert Kirchhoff)和罗伯特·本森(Robert Bunsen)通过观察元素燃烧时形成的光谱指出,每种化学元素的辐射都有独特的“特性”,并推断出太阳中的暗线光谱是由太阳上层元素的吸收引起的。有些东西会被地球大气中的氧分子吸收。例如,我们可以通过光谱仪观察正在燃烧的氢气来观察一组不同的辐射。

氢的辐射
比较看这两张图,不难看出这两条线是一致的。在实验过程中,基尔霍夫和本生观察了太阳通过高温气体(来自本生灯)时的光谱,并比较了不同元素发出的光谱。本生灯就是在这个过程中发明的。
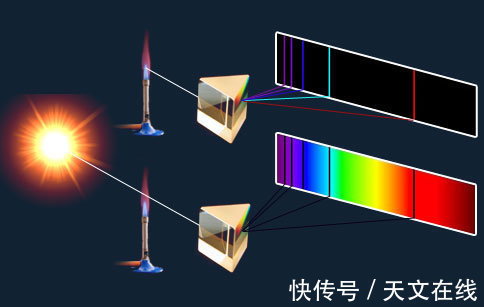
Kirchoff-Bunsen 实验
一般来说,太阳光谱中有超过 1,000 条可观测的弗劳恩霍夫光谱线。因为每个元素都有自己的特性,我们可以通过分析光谱线来推断太阳或任何未知的事物。物体的化学成分。
那么是什么造成了这种现象呢?
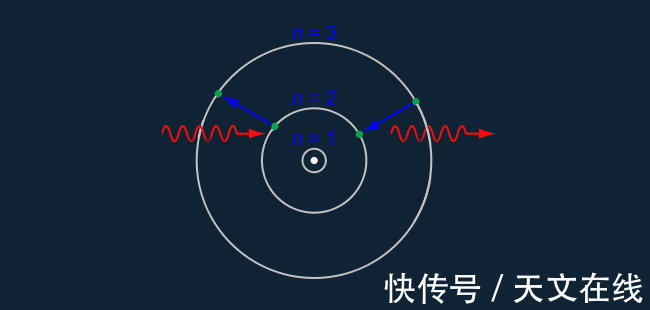
电子能级
原子它由质子、中子和电子组成。质子带正电,电子带负电,中子不带电(电中性)。丹麦物理学家 Niels Bohr 设计了一个有助于解释吸收线和发射线的原子模型。在他的模型中,质子和中子在原子核中,电子围绕原子核运行。值得注意的是,在这个模型中,电子只能在离原子核一定距离的地方运行,就像行星只能在一定距离内绕太阳运行一样。离原子核越远,需要的能量就越多。每个“距离”称为一个能级。电子可以在不同能级之间移动,但需要进行能量交换。当我们谈论光子的能量时,我们也可以谈论波长,因为两者是相关的。所需的能量是由两个能级之间的能量差决定的,不同能级和不同元素的不同能级是不同的。将元素组合成分子也会改变能量需求。
光子的能量公式:

频率公式:
< p>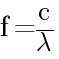
C 是光速 (3x108?ms-1),λ 是波长,单位是赫兹。
电子要移动到更高的能级,它必须获得能量。一种方法是吸收具有适当能量的光子。当电子吸收光子时,对应的波长似乎从光谱中消失了。因为它已经被吸收了。相反,当电子移动到较低的能级时,它会释放相同数量的能量,从而产生发射线。能级一般为记为n,第一个能级为n=2(对于原子核,n=1)。从n=2到n=3需要能量吸收,从n=3t o n = 2 释放能量。回到我们的氢原子,当它来自一个太阳光子获得能量,一个电子从n=2跃迁到n=3,形成一条吸收线。当我们在燃烧器中加热氢气时,我们实际上用能量激活了电子,然后它再次释放能量。当电子回到 n = 2 时。电子可以从 n = 2 跳到 n = 3,或者跳到 n = 4、5 等。下表总结了氢所需的能量。这也称为鲍尔默系列。
文章来源:《光谱学与光谱分析》 网址: http://www.gpxygpfxzz.cn/zonghexinwen/2021/0818/470.html